با واکسینه شدن ۶۵ درصد افراد بالای ۱۲سال در کشور، تولیدکننده های جدید واکسن کرونا در ایران، با کاهش جمعیت داوطلب و کندی کارآزمایی بالینی مواجه شدهاند. مشاور وزیر بهداشت میگوید: تعداد بالای تولید واکسن های داخلی توجیه پذیر نیست و در آینده احتمالا واکسنهای داخلی کرونا با هم ادغام میشوند.
به گزارش کرج رسا به نقل از همشهری؛ ماراتن تولید واکسنهای داخلی با افزایش واردات و تزریق ۶۵درصدی جمعیت بالای ۱۲سال کشور سختتر شده است. از مجموع جامعه ۶۸میلیون نفری بالای ۱۲سال ایران که اکنون واکسن دریافت میکنند تا ظهر دیروز ۴۴میلیون و ۳۷۸ هزار و ۲۳۴ نفر دوز اول و ۱۸میلیون و ۶۰۰ هزار و ۵۵۴ نفر نیز دوز دوم را تزریق کردهاند تا مجموع واکسنهای تزریق شده در کشور به ۶۲میلیون و ۹۷۸ هزار و ۷۸۸ دوز برسد.
حالا بهنظر میرسد که واکسیناسیون ۷۵ درصدی جامعه بهزودی محقق میشود اما همین اتفاق نگرانیهایی برای ورود به کارآزمایی بالینی واکسنهای جدید ایجاد کرده است. با کاهش ظرفیت جمعیت دریافتکننده واکسن، همین حالا هم روند کارآزماییهای بالینی کندتر از قبل شده و به تأکید برخی متولیان واکسنهای داخلی روند کند صدور مجوزها و نبود سازوکار مشخص در ورود برخی واکسنها به سبد مصرف واکسیناسیون کشور احتمالا به تخریب پروژههای ایرانی – ملی واکسنهای کرونا در کشور و دلسردی دیگر تولیدکنندگان منجر خواهد شد.
همه اینها در شرایطی است که تا همین حالا هم واکسنهای وعده داده شده برای تولید میلیونی، با مشکل در مواجه شدهاند. واکسن برکت قرار بود تا پایان تابستان ۱۴۰۰، ۵۰میلیون دوز واکسن تولید کند اما تاکنون تنها حدود ۶میلیون دوز از این واکسن به وزارت بهداشت تحویل داده شده است، آن هم درحالیکه زمستان سال گذشته مصطفی قانعی، رییس کمیته علمی ستاد ملی مقابله با کرونا از فراهم شدن مقدمات ساخت واکسنهای مختلف کرونا در ایران خبر داده و گفته بود که «تا شهریور ۱۴۰۰واکسن ایرانی کرونا در انواع مختلف به مرحله تولید میرسد و ایران قطب تولید واکسن در دنیا میشود.»
این در حالی است که مجموع واکسنهای تحویل داده شده از سوی تولیدکنندههای داخلی به وزارت بهداشت، به ۱۵میلیون دوز هم نرسیده و بیشترین نیاز کشور از واردات واکسنهای خارجی تامین شده است. اکنون از میان ۹واکسن ایرانی که موفق شدند مجوزهای سازمان غذا و دارو برای انجام کارآزماییهای بالینی را بهدست بیاورند، تنها دو واکسن کووایران برکت، پاستوکووک به مرحله تزریق عمومی رسیدهاند.
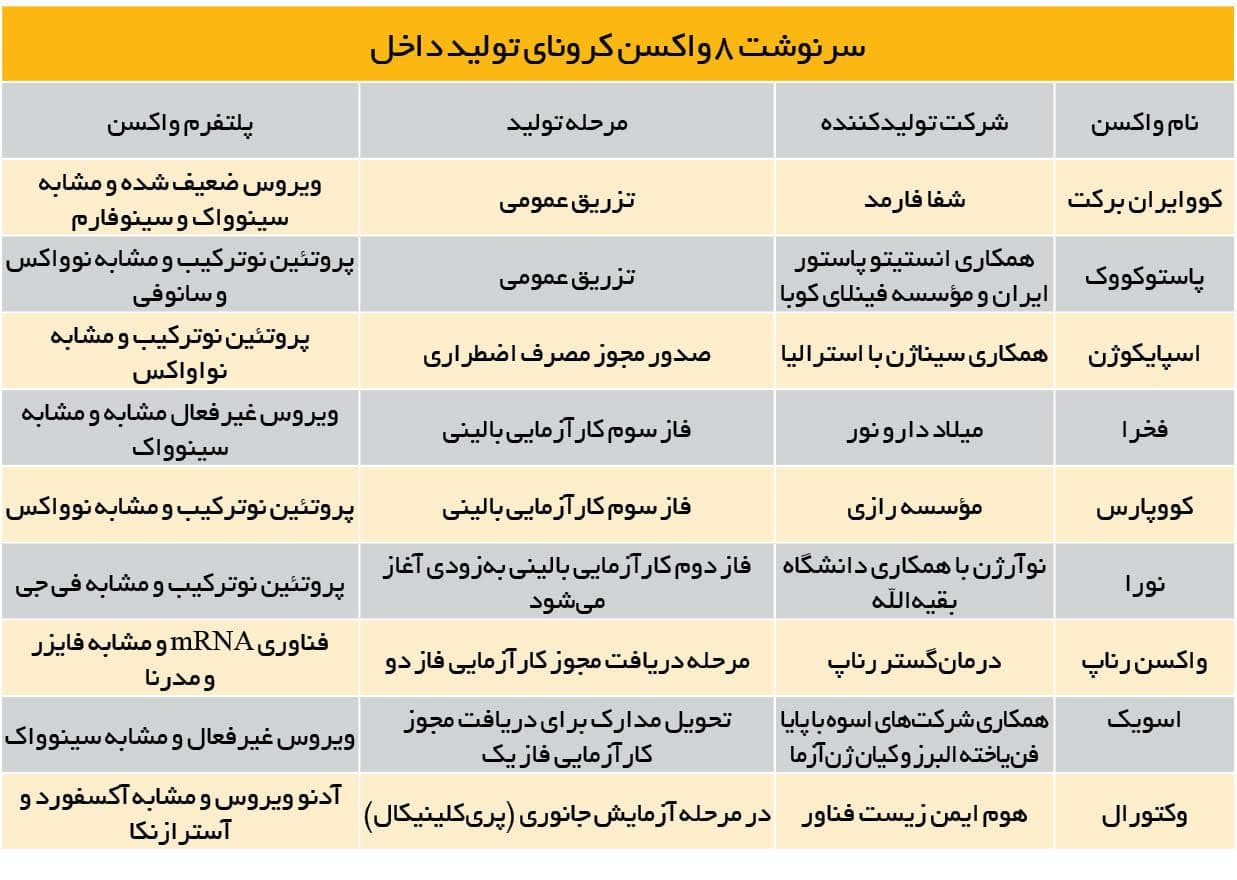
واکسن اسپایکوژن چند روز پیش مجوز مصرف اضطراریاش را دریافت کرده و کارآزمایی ۶واکسن دیگر ازجمله فخرا، کووپارس، نورا، mRNA رناپ، وکتورال و اسویک هنوز به پایان نرسیده و با وجود کاهش جمعیت هدف برای انجام کارآزماییهای چند ۱۰هزار نفره به نظر می رسد خط پایان مطالعات این واکسنها طولانیتر از پیشبینیهای گذشته باشد. هر چند بهگفته متولیان واکسنهای ایرانی، براساس اعلام سازمان غذا و دارو قرار است واکسنهای با پلتفرم مشابه با دیگر واکسنهای مجوز گرفته زودتر از زمان تکمیل کارآزماییها مجوز مصرف اضطراریشان را دریافت کنند و به سبد واکسیناسیون افزوده شوند.
سرنوشت ۹ واکسن ایرانی
ماههاست که وعده تولید و تحویل انبوه واکسن برکت شنیده میشود اما هنوز میزان تحویل آن به وعدههای داده شده، نرسیده است. براساس اعلام رسمی وزارت بهداشت تا پایان شهریور تنها ۶میلیون دوز از این واکسن برکت به وزارت بهداشت تحویل داده شده است. همچنین علیرضا بیگلری، رییس انستیتوپاستور ایران صبح دیروز در نشست خبری مجازی درباره تولید انبوه پاستوکووک گفت: «از شنبه هفته گذشته یک میلیون و ۲۰۰هزار دوز از یک بچ بیش از شش میلیونی را تحویل وزارت بهداشت دادیم. اواخر این هفته مجددا حدود یک میلیون دوز از همین واکسن تقدیم وزارت بهداشت میشود. تولید و تحویل واکسن طوری برنامهریزی شده که بهطور متوسط هفتهای حداقل یک میلیون دوز را داشته باشیم.»
مجوز مصرف اضطراری واکسن کرونای اسپایکوژن بهعنوان نخستین واکسن بخش خصوصی ایران هم هفته گذشته صادر شد. بهگفته هاله حامدیفر، مدیرعامل شرکت سیناژن هماکنون یکمیلیون و ۷۰۰هزار دوز از این واکسن آماده تحویل است و ظرفیت تولید این واکسن هم بهصورت ماهانه سهمیلیون دوز خواهد بود. حامدیفر از اجرای کارآزمایی بالینی اسپایکوژن برای ۱۷هزار نفر خبر میدهد و به همشهری میگوید: «با صدور مجوز اضطراری، این واکسن به سبد واکسیناسیون کشور اضافه خواهد شد. البته کارآزمایی بالینی این واکسن مطابق با پروتکل وزارت بهداشت با مونیتور کردن کلیه افرادی که در کارآزمایی شرکت کردند همچنان ادامه دارد.» مدیرعامل شرکت سیناژن درباره چالشهای انجام کارآزماییها در مقطع کنونی و با توجه به کاهش جمعیت واکسینه نشده هم میگوید: «قطعا این شرایط برای شرکتهایی که بهتازگی کارآزماییهایشان را آغاز میکنند، سختتر است اما هماکنون شاهد یک رویه دیگر هستیم و مطالعات بالینی بهصورت مقایسهای با دیگر واکسنهای موجود در بازار انجام میشود. این مسئله میتواند تا حدودی باعث تسهیل در این شرایط شود.»
فخرا و کووپارس؛ یک قدم تا مجوز اضطراری
واکسن فخرا اما فاز سه کارآزمایی را به شکلی متفاوت پیگیری میکند و در این مرحله سازندگان آن اقدام به تزریق واکسننما یا پلاسبو به داوطلبان نخواهند کرد. براساس اعلام مسئولان این شرکت در این مطالعه داوطلبان بهصورت تصادفی یکی از واکسنهای فخرا و سینوفارم را دریافت خواهند کرد، امکان دریافت واکسن بهصورت غیرتصادفی (انتخاب یکی از دو واکسن فخرا یا سینوفارم) هم برای آنها فراهم شده است. هر چند بهنظر میرسد کارآزماییهای بالینی این واکسن کندتر از حد انتظار پیش میرود و آنها یکی از شرکتهایی هستند که احتمالا برای تکمیل جامعه هدف داوطلب ۴۶هزار نفری برای تزریق واکسن با مشکل کمبود مراجعهکنندگان مواجه باشند. اتفاقی که درباره واکسن کووپارس رازی هم در فاز سوم کارآزمایی بالینی افتاد؛ واکسنی که اکنون در تهران و البرز در حال تزریق است اما بخش عمده آن در البرز تزریق شده است. گفته میشود، آمار واکسنهای تزریق شده کووپارس رازی در مرحله فاز سوم کارآزمایی بالینی به بیش از ۱۴هزار دوز رسیده است. هر چند براساس پروتکلهای کارآزمایی این عدد باید به ۴۰هزار نفر برسد اما بهگفته یکی از مسئولان این شرکت براساس وعده وزیر بهداشت دولت دوازدهم با توجه به مشابه بودن پلتفرم این واکسن با دیگر واکسنهای ویروس ضعیف شده قرار بود با عبور تزریق از مرز ۱۰هزار نفر مجوز مصرف اضطراری برای کووپارس هم مانند دیگر واکسنها صادر شود. اما این اتفاق تاکنون رخ نداده است. حالا با تأخیر در صدور مجوز مصرف اضطراری احتمالا تداوم کارآزماییها هم با چالش کمبود داوطلبان مواجه باشد . اواخر هفته گذشته علی اسحاقی، رییس مؤسسه تحقیقات واکسن و سرمسازی رازی از توقف تولید این واکسن خبر داد و گفت: «تاکنون بیش از ۲میلیون دوز واکسن کرونای رازی تولید شده اما این واکسن هنوز مجوز مصرف اضطراری را دریافت نکرده به همین دلیل فعلاً روند تولید آن متوقف شده است.»
«نورا» در راه کارآزمایی فاز ۲
در این میان فاز دوم کارآزمایی بالینی واکسن نورا هم بهزودی آغاز خواهد شد و بهگفته غلامرضا اولاد، مجری طرح واکسن نورا در فاز۲مشکل خاصی برای تزریق واکسن به گروه داوطلب وجود نخواهد داشت؛ «هر واکسنی برای کسب مجوز مصرف اضطراری ناگزیر باید کارآزماییها بالینی را طی کند در دوز دوم فاز بالینی عدد قابل توجهی لازم نیست و مشکل خاصی در اینباره وجود ندارد. در این مرحله ما ۳۰۰داوطلب را تحت مطالعه قرار خواهیم داد و قطعا برای ورود به کارآزمایی فاز۳ وزارت بهداشت و سازمان غذا و دارو تدابیر جدید در اینباره خواهند داشت.» بهگفته اولاد، با توجه به اینکه جمعیت واکسینه شده کشور بهسرعت در حال افزایش است، سیاستگذاری کلان سازمان غذا و دارو و وزارت بهداشت هم تحتتأثیر قرار خواهد گرفت و با توجه به اهمیت پروژه ملی واکسنهای ایرانی در اینباره تدابیری اندیشیده خواهد شد؛ «واردات واکسن با هدف واکسیناسیون هر چه سریعتر مردم همچنان در حال انجام است اما رگولاتوری هم جزو سیاستهای وزارت بهداشت خواهد بود و بهطور حتم تمهیدات جدید برای تیمهای داخلی مطالعات واکسن درنظر گرفته میشود.»
«رناپ» و «اسویک» در انتظار کارآزمایی ها
در میان تمام واکسنهای تولید داخل، واکسن mRNA رناپ هماکنون در انتظار دریافت مجوز کارآزمایی فاز ۲است. بهگفته مصطفی قانعی، عضو کمیته ملی واکسن کرونا این واکسن پروندهاش را تحویل داده و ایراداتی از آن گرفته شده که با رفع آن مجوزهای لازم صادر خواهد شد. اسویک واکسن ایرانی با پلتفرم مشابه برکت و سینوفارم هم در انتظار صدور مجوز از سوی سازمان غذا و دارو برای شروع کارآزمایی بالینی فاز یک است. درباره این واکسن هم با وجود تأخیر در آغاز کارآزماییهایی بالینی و همان چالشهای کمبود جمعیت داوطلب اما ظرفیت ادغام و دریافت مجوزهای زودهنگام بهدلیل پلتفرمهای مشابه مطرح میشود. در نهایت نهمین واکسن ایران ، وکتورال هم دیگر واکسنی است که هنوز کارآزماییهای مرحله جانوری (پریکلینکال) آن به پایان نرسیده است.
تعداد بالای تولید واکسن های داخلی توجیه پذیر نیست
حسین وطنپور، عضو هیأت علمی دانشکده داروسازی دانشگاه شهید بهشتی و مشاور وزیر در امور اجرایی واکسنهای داخلی کووید-۱۹، ایجاد اختلال در کارآزمایی بالینی تولیدات جدید واکسن را تأیید میکند اما به همشهری میگوید که این موضوع، مشکل تولیدکنندههای جدید واکسن کروناست . زمانی که برای تولید واکسنها از روشهای یکسانی استفاده میشود، ۸۰تا۹۰درصد میتوان گفت که اثرات مشابهی هم دارند. بنابراین از روش بیوسیمیلار استفاده میشود. این اتفاق برای داروها هم میافتد. یعنی زمانی که یک محصول در خارج از کشور تولید میشود و تمام تستهای بالینی را هم میگذراند، وقتی در داخل تولید میشود، دیگر نیازی به گذراندن تستهای بالینی ندارد. البته به شرطی که تمام فرایند تولید آنها یکسان باشد، بنابراین کارایی آنها مقایسه و به همان بسنده میشود. او میگوید: «زمانی که تولیدکننده جدیدی میگوید که میخواهم از ویروس ضعیف شده برای تولید واکسن استفاده کند، اگر فرایند تولید آن با سایر واکسنها یکسان باشد، دیگر نیازی به تکرار کارآزمایی بالینی نیست.»
هماکنون ۹ واکسن کرونا در داخل تولید میشود اما در نوزدهمینماه از شیوع کرونا در ایران، جز واکسن برکت، آن هم بهطور محدود، واکسنهای دیگر، جایگاه ویژهای در سبد واکسیناسیون نداشتهاند. حالا سؤال اینجاست که تولید این میزان واکسن کرونای داخلی چه توجیهی دارد؟ وطنپور در اینباره معتقد است که تولید این میزان واکسن داخلی، توجیهپذیر نیست. او میگوید: «بسیاری از واکسنهایی که در حال تولیدند، در آینده در هم ادغام میشوند، در دنیا هم مرسوم است که واکسنها با هم ادغام شوند.»
این مسئول در وزارت بهداشت در ادامه درباره سرنوشت واکسن برکت هم توضیحهایی میدهد. او میگوید که در اعلام زمان تولید و توزیع و حتی میزان تولید این واکسن عجله شد؛ «تولید واکسن، مشابه تولید محصولات دیگر نیست. واکسن بعد از تولید باید دو هفته مورد آزمایش قرار گیرد و تستهای متعددی روی آن انجام شود. گاهی این واکسنها در آزمایشها نمره قبولی نمیگیرند.
اگر واکسنی حتی درصورت نتیجه بخش بودن در کارآزمایی بالینی، پس از تولید نتواند سیستم ایمنی را تحریک کند، از پروسه تولید خارج میشود. گاهی ممکن است در خط تولید مشکل ایجاد شود.ما پتانسیل تولید واکسن را داریم اما برای اینکه بتواند وارد بازار شود با چالشهایی مواجهیم.»
































لطفا از نوشتن با حروف لاتین (فینگلیش) خودداری نمایید.
از ارسال دیدگاه های نامرتبط با متن خبر،تکرار نظر دیگران،توهین به سایر کاربران و ارسال متن های طولانی خودداری نمایید.
لطفا نظرات بدون بی احترامی ، افترا و توهین به مسٔولان، اقلیت ها، قومیت ها و ... باشد و به طور کلی مغایرتی با اصول اخلاقی و قوانین کشور نداشته باشد.
در غیر این صورت مطلب مورد نظر را رد یا بنا به تشخیص خود با ممیزی منتشر خواهد کرد.